L’eau, cette inconnue
1. L’eau est-elle une anomalie de la nature ?
L’eau, l’élément le plus abondant de notre biosphère, au cœur de la plupart de phénomènes biologiques demeure en partie un mystère pour la physique contemporaine. Ses propriétés dans des conditions usuelles de température et de pression le fond apparaître unique et extraordinairement apte à sa fonction de solvant. Et très étonnamment ses propriétés à basse température font l’objet de nouvelles controverses.

Principales anomalies de l’eau :
– très forte cohésion, qui se traduit par des températures de fusion et d’ébullition élevées ;
– constante diélectrique élevée, qui lui permet de dissoudre tous les sels ;
– grande expansion à basse température (en dessous de 4°C) et aussi lors de la cristallisation.
Si on regarde les éléments qui suivent directement l’oxygène – l’eau est de formule chimique H2O, un atome d’oxygène lié à deux atomes d’hydrogène – dans la classification périodique pour essayer de savoir sous quelle forme est l’eau à température ambiante, alors tout laisse à penser qu’elle doit être gazeuse, comme l’est, par exemple, le sulfure d’hydrogène, de formule H2S.
La liaison hydrogène s’établit entre deux molécules identiques ou non. C’est le déficit de charge portée par l’atome d’hydrogène qui permet l’apparition de la liaison.
L’agitation thermique caractérise le mouvement des particules (atomes, molécules…). La température est une mesure de cette agitation.
L’eau n’est pas un gaz à température ambiante, parce que les liaisons hydrogène sont suffisamment fortes. L’eau est donc douée d’une grande force de cohésion. Résultat : il faut apporter beaucoup d’énergie pour rompre ces liaisons, ce qui explique qu’elle ne bout qu’à 100 °C. De l’autre, ce n’est pas non plus un solide à température ambiante, parce que les liaisons sont tout de même fragiles.
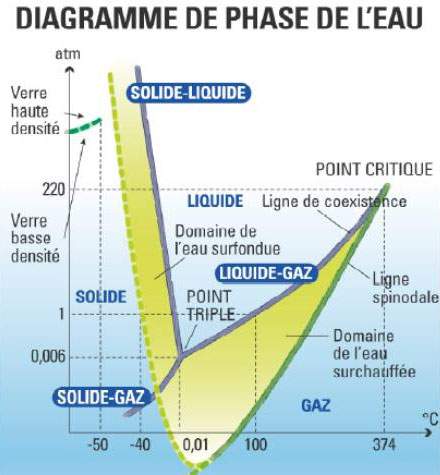
Si l’eau se cristallise en glace couramment à 0°C, dans le cas extrême d’une eau pure surfondue dont la température est progressivement abaissée à -40°C, l’agitation thermique des molécules d’eau sous ce seuil n’est plus suffisante pour éviter que le liquide ne se transforme en glace. Passée cette barrière de température, la durée de vie de l’eau liquide devient extrêmement brève. Les physiciens n’ont alors plus le moyen de l’observer.
C’est aux alentours de -130°C qu’apparaît un autre phénomène intéressant : si l’eau est refroidie suffisamment vite jusqu’à cette température, elle se transforme en glace amorphe, c’est-à-dire qu’elle a la structure du verre.
2. Structure microscopique
L’eau est le seul corps plus dense à l’état liquide qu’à l’état solide. L’énergie nécessaire pour la porter à ébullition ferait fondre la casserole si cette dernière était vide. De l’eau ultra propre peut rester liquide jusqu’à +220°C sans bouillir et jusqu’à -40°C sans geler.
La cause de ces remarquables propriétés ? La liaison hydrogène. Au contraire des liaisons covalentes 50 fois plus fortes qui lient dans chaque molécule l’oxygène à deux atomes d’hydrogène, elle ne lie pas entre eux des atomes de la même molécule mais des atomes de molécules proches. Et c’est cette liaison faible qui est responsable des propriétés remarquables de l’eau. A température ambiante l’énergie de la liaison hydrogène de 10Kjoules par mole est quatre à cinq fois supérieure à l’énergie thermique (l’énergie cinétique) des molécules.

L’eau serait donc solide ? Heureusement pas car ces liaisons sont directionnelles ; dès que l’axe reliant les atomes O-H-O s’écarte des 30°, la liaison se rompt. Or cette liaison maintient les molécules éloignées de 0,18 Angström contre 0,10 A pour la liaison covalente O-H ; les molécules peuvent se rapprocher. C’est pour cette raison que la glace transformée en liquide à la température de 0°C voit sa densité augmenter jusqu’à 4° ; entre 0 et 4°C, plus les liaisons hydrogène e rompent, plus l’eau devient dense. Puis au-delà l’agitation thermique repousse les molécules et l’eau devient moins dense.
Pour passer de 0 à 100°C il faut rompre en moyenne une liaison par molécule. Or une molécule d’eau pouvant participer à 4 liaisons hydrogène elle n’a moins de voisines que la dizaine couramment dans d’autres corps ; l’eau possède plus de volume libre pour absorber les vibrations internes à chaque molécule d’eau, d’où sa grande capacité calorifique.
L’eau est un liquide associé, c’est-à-dire que les liaisons intermoléculaires sont prépondérantes. Ces liaisons hydrogène sont attractives du fait des polarités opposées des atomes d’oxygène et d’hydrogène. Elles se forment et se défont en un millième de milliardième de seconde, une durée remarquablement indépendante de la température. A cette fréquence d’observation l’eau apparaît comme un solide et une onde sonore de fréquence très élevée s’y propage comme dans une onde dans un solide, perturbant les molécules de proche en proche.
L’eau surfondue se transforme en cristal de glace dès qu’une micropoussière y est introduite ou si le récipient contient la moindre aspérité, on parle de nucléation. Ce corps étrange sert d’ancrage aux premières molécules ordonnées qui constituent l’amorce. En dessous de -40°C, la très faible agitation thermique ne permet plus d’empêcher la formation de petites zones de densité égales à celles de la glace cristalline ; l’eau ne peut plus être liquide. Et au contraire des autres corps dont les propriétés divergent lors de la transition vitreuse, c’est à ce seuil de nucléation que l’eau possède des propriétés divergentes de compressibilité, de capacité calorifique et de viscosité. Cette absence d’écoulement, cette viscosité infinie, ne se produit pas à l’état vitreux mais au passage en phase cristalline. Et comprendre cette phase de transition de l’eau surfondue s’avère très difficile car à cette température la transition est extrêmement rapide.
Le nombre de liaisons hydrogène augmente quand la température baisse ; les molécules d’eau se déplacent de moins en moins vite. Les liaisons formant un cristal de mailles tétraédriques, la viscosité augmente fortement lors de cette cristallisation. Mais pourquoi à -40°, si loin de la transition vitreuse à -135°C, l’eau se fige non pas comme un cristal régulier mais comme un liquide que l’on aurait brutalement figé.
Mais si l’eau peut rester surfondue jusqu’à -40°C dans des conditions de pureté qui lui évite de se transformer en glace cristalline, ses propriétés entre -40° et -135°C nouveau seuil, celui de la transition vitreuse, s’explique difficilement par la seule liaison hydrogène mais nécessite d’introduire des notions d’interactions à plus large échelle.
II existe en effet une glace vitreuse à haute densité produite à haute pression (12000 atmosphères et à -196°C) dont la densité est 30% supérieure à la glace ordinaire car une partie des liaisons hydrogène se sont rompues et cette densité subsiste lorsque l’on revient à la pression ordinaire.

Il est envisagé que la glace entre -40 et -135°soit une combinaison de deux formes de glace haute et basse densité ; la glace à haute densité subsistant sous formes métastable au-dessus du seuil de -135°C de transition vitreuse, tout comme l’eau surfondue existe jusqu’-40°C.
Une autre possibilité est que les molécules d’eau à plus grande échelle pourraient se comporter comme des polymères avec une température de transition vitreuse, les liaisons hydrogènes formant des sortes de rameaux latéraux à ces polymères dont les mouvements déterminent le comportement de l’eau entre -40 et -135°C.
L’eau est en bon exemple d’un élément dont les facteurs physiques qui entrent en jeu dans la caractérisation de ses propriétés dépendent de l’échelle considérée.
Au niveau de sa description courante, les propriétés de l’eau sont caractérisées par trois facteurs : sa densité, sa viscosité et son indice diélectrique (ou indice optique).
La densité est légèrement fonction de la température. Mais pour rendre compte de ce facteur, il faut modéliser l’eau comme un amalgame de molécules d’eau dont le volume propre n’est pratiquement pas fonction de la température. L’amalgame des molécules d’eau n’est possible que grâce à la polarisation naturelle de l’eau. Ce facteur n’entre en jeu qu’à l’échelle des molécules.
Or ces molécules peuvent se briser sous la température ou par les chocs. La polarisation est donc le produit de l’assemblage des atomes dans la molécule ; c’est la polarisabilité, facteur à l’échelle atomique.
On peut réduire encore l’échelle et voir la polarisabilité comme le produit des nombres quantiques qui attribuent aux atomes d’hydrogène et d’oxygène des capacités de liaison lié à la forme géométrique des orbitales de leurs électrons. Ces nombres sont n pour nombre quantique principal (niveau d’énergie), l pour le nombre quantique orbital (longueur du moment de la quantité de mouvement), m pour nombre quantique magnétique (projection de ce moment sur une droite ou axe de mesure).
Un des principaux objectifs expérimentaux est d’améliorer les expériences dites de cavitation, qui se déroulent à température ambiante et à des pressions qualifiées de « négatives ». Elles mettent à l’épreuve la cohésion de l’eau en recherchant la traction maximale qu’on peut exercer avec des ultrasons sur de l’eau liquide avant que la première bulle de vapeur ne se forme. L’espoir est d’atteindre une pression de -1400 bars. Alors des éléments nouveaux qui permettraient d’écarter certaines hypothèses sur la structure de l’eau.
On a atteint -400 bars dans de l’eau propre mais pas particulièrement dégazée. La méthode utilisée permet d’étudier la cavitation sur un temps court (100 nsec) et dans un volume réduit (une fraction de la longueur d’onde acoustique au cube) ; elle est donc moins sensible aux traces de gaz dissous que les méthodes précédemment utilisées. Il devrait suffire d’utiliser un amplificateur cinq fois plus puissant (environ 1kWatt) pour atteindre l’extrême limite de métastabilité prévue à -2100 bars dans l’eau à 30°C.
L’apparition explosive d’une bulle s’appelle la cavitation. Une chute de pression est équivalente à un chauffage de l’eau. Les chercheurs étirent l’eau (ils parlent de pression négative) jusqu’à observer la première bulle de vapeur.
Quelle est la limite extrême de stabilité de l’eau pure à pression négative ?
La limite spinodale de l’eau est minimale (- 2100 bars) à 30°C, et remonte à – 1800 bars à 0°C avant de rejoindre une autre limite spinodale, celle qui concerne la métastabilité de l’eau par rapport à la nucléation de la glace. La remontée de la spinodale liquide-gaz est liée au fait qu’il est impossible de maintenir l’eau liquide en surfusion au-delà de -45°C. C’est lié aussi au fait que le coefficient de dilatation thermique change de signe de part et d’autre d’une ligne de maxima de densité dont la forme exacte n’est pas connue à pression très négative.
3. Illustration : pourquoi l’eau gèle en surface des lacs ?
Il se trouve que l’eau a sa densité maximale à 4°C et qu’elle diminue entre 4°C et 0°C. La glace a une densité de 0,92 gramme par cm3. La surface de l’eau cède de la chaleur à l’air ambiant jusqu’à ce qu’elle atteigne 4°C. Etant à sa densité maximale, elle est entraînée vers le fond. La masse entière se refroidit, processus d’autant plus long que le lac est profond. Cela explique que les flaques d’eau gèlent bien avant les étangs. Dès que la température descend en dessous de 4°C l’eau de surface, moins dense que l’eau de profondeur, reste en haut où elle va se refroidir jusqu’à 0°C avant de geler. La couche de glace s’épaissit pendant que le reste de l’eau reste à 0°C permettant la vie aquatique en hiver. Le processus ralentit car la glace est un isolant thermique (igloo). La chaleur de l’eau qui se trouve en dessous a de plus en plus de difficulté à être évacuée. La vitesse de formation d’une couche de glace est inversement proportionnelle à son épaisseur ; lorsque l’eau se solidifie ou que la glace fond, la température reste constante à 0°C et seule la quantité de glace varie.
yogaesoteric
10 mai 2019
Also available in:

