Le sommeil : faire la lumière sur notre activité nocturne (1)
Une fonction encore mystérieuse, mais déterminante pour la santé : Les gens passent près d’un tiers de leur vie assoupi. Mémoire et apprentissage, métabolisme, immunité… même si beaucoup d’hypothèses doivent encore être confirmées, et si d’autres ne manqueront pas d’être formulées, il est parfaitement établi que le sommeil est crucial pour de nombreuses fonctions biologiques. L’enjeu est de taille : la fréquence des troubles du sommeil, qui touchent une part importante de la population, a augmenté ces dernières décennies. Elle interroge l’évolution à venir de notre état de santé.
Les enjeux de la recherche : Parce que le sommeil influence la santé et les risques d’accidents, il est essentiel de comprendre ce qui en détermine précisément la qualité ou la durée. Avec l’essor des neurosciences, les progrès s’accélèrent. De quoi affirmer, encore plus fermement, l’importance d’une bonne nuit de sommeil.

Le sommeil correspond à une baisse de l’état de conscience qui sépare deux périodes d’éveil. Il est caractérisé par une perte de la vigilance, une diminution du tonus musculaire et une conservation partielle de la perception sensitive.
Lent, profond, paradoxal, les visages du sommeil sont multiples
Schématiquement, le sommeil correspond à une succession de 3 à 6 cycles successifs, de 60 à 120 minutes chacun. Un cycle est lui-même constitué d’une alternance de sommeil lent et de sommeil paradoxal, correspondant chacun à une activité cérébrale différente mise en évidence par électroencéphalographie (EEG) : sur le tracé, les ondes électriques qui parcourent le cerveau et qui témoignent de l’activité neuronale ont un aspect différent selon la phase de sommeil. Lors de la phase d’éveil, par exemple, elles sont courtes et fréquentes.
Le sommeil lent porte ce nom car il est caractérisé par des ondes lentes. Il comporte lui-même plusieurs stades : après une phase de transition (N1) de quelques minutes, séparant la veille et le sommeil, la phase de sommeil léger (N2) s’installe. Elle est suivie par une phase de sommeil progressivement plus profond (N3) qui dure plusieurs dizaines de minutes. Pendant cette période, l’EEG montre la présence d’ondes de grande amplitude et de faible fréquence. L’imagerie fonctionnelle montre une consommation en oxygène réduite et donc un métabolisme cérébral ralenti. Le tonus musculaire est lui-aussi diminué, mais encore partiellement présent, pouvant expliquer les épisodes de somnambulisme (voir plus loin).
Le sommeil paradoxal correspond à une période durant laquelle l’activité cérébrale est proche de celle de la phase d’éveil. Il est aussi appelé période REM (Rapid Eye Movement), en raison de fréquents mouvements oculaires rapides (sous les paupières fermées). A l’inverse, le tonus musculaire est totalement aboli durant cette phase, en dehors de quelques mouvements des extrémités. Parallèlement, la pression artérielle et le rythme respiratoire connaissent de fréquentes fluctuations. Le sommeil paradoxal est en outre propice aux rêves : il regroupe les rêves les plus intenses et ceux dont on peut garder le souvenir une fois éveillé. Des rêves peuvent aussi survenir au cours du sommeil lent léger, mais ils sont moins intenses et correspondent moins à une représentation onirique de réalisations ou d’actions qu’à des idées abstraites.
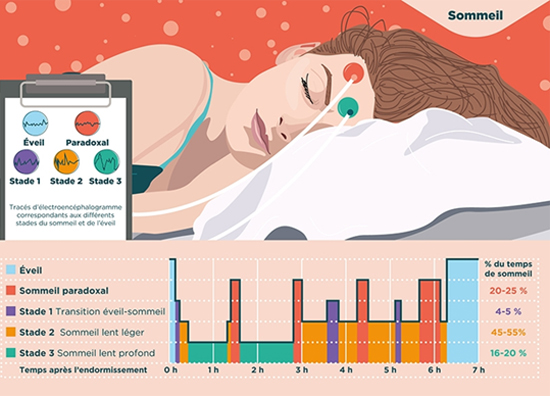
Infographie illustrant les différents stades du sommeil et de l’éveil enregistrés sur un sujet, par électroencéphalogramme, pendant la nuit. Le sommeil se compose du sommeil paradoxal, de la transition éveil-sommeil (stade1), du sommeil lent léger (stade2) et du sommeil lent profond (stade3). Au fur et à mesure de la nuit, le sommeil lent profond diminue au profit du sommeil lent léger.
Le rythme de sommeil n’est jamais figé
Le rythme de sommeil varie en premier lieu au cours d’une même nuit : schématiquement, les premiers cycles sont essentiellement constitués de sommeil lent profond, tandis que la fin de nuit fait la part belle au sommeil paradoxal. Et si la nuit précédente a été mauvaise, le sommeil lent sera d’autant plus profond la nuit suivante.
Le sommeil varie également au cours de la vie : le sommeil lent est plus profond durant la croissance, jusque vers l’âge de 20 ans environ. A mesure que l’on vieillit, celui-ci devient minoritaire et laisse la place à un sommeil lent, plus léger, expliquant l’augmentation des troubles du sommeil avec l’avancée en âge. Parallèlement, le sommeil paradoxal est plus long dans les premières années de vie. Sa durée se réduit à l’âge adulte.
Enfin, la quantité nécessaire et la qualité de sommeil varient grandement d’une personne à l’autre. L’environnement, l’hygiène et le rythme de vie jouent un rôle sur la capacité à dormir et bien récupérer lors d’une nuit de sommeil. La génétique aiderait quant à elle à différencier les lève-tôt des couche-tard, ou les gros des petits dormeurs. Les petits dormeurs présenteraient notamment des phases de sommeil léger très courtes. Mais quelle que soit la durée de sommeil nécessaire à chacun, celle du sommeil profond, phase du sommeil primordiale pour le repos de l’organisme, caractérisé par une baisse de l’activité physiologique et cérébrale serait relativement constante, tandis que les durées de sommeil léger et de sommeil paradoxal varieraient.
Comment étudie-t-on le sommeil ?
L’examen de référence est la polysomnographie. Il permet d’obtenir un hypnogramme, c’est à dire un enregistrement de plusieurs paramètres, obtenu à l’aide d’électrodes placés au niveau du crâne et de différentes parties du corps : l’activité cérébrale (par EEG), l’activité musculaire (électromyogramme) et les mouvements oculaires (électro-oculogramme). Ces données vont permettre de suivre et d’identifier les différentes phases de sommeil. Parallèlement, le rythme cardiaque, le rythme respiratoire et les mouvements des jambes sont également enregistrés afin de caractériser certains troubles ou certaines pathologies nocturnes.
D’autres approches sont utilisées afin d’explorer les troubles du sommeil : un agenda du sommeil permet aux personnes concernées de consigner leurs habitudes de sommeil et d’éveil, de coucher et de lever, pour mieux décrire d’éventuelles insomnies. L’actimétrie, qui enregistre les mouvements corporels grâce à un bracelet porté au poignet, permet également de mieux caractériser les alternances veille-sommeil au cours de la journée. Par ailleurs, des tests itératifs de latence d’endormissement (TILE) sont indiqués dans l’exploration de la narcolepsie et des tests de maintien d’éveil (TME) le sont pour évaluer la somnolence diurne et la propension au sommeil.
Enfin, les techniques d’imagerie médicale (IRM, scanner), et a fortiori celles d’imagerie fonctionnelle (PET scan, IRM fonctionnelle, technique d’imagerie médicale utilisée pour étudier le fonctionnement du cerveau, magnétoencéphalographie), offrent aux chercheurs les moyens d’étudier précisément les caractéristiques et le rôle de chacune des phases de sommeil, tout en identifiant les structures cérébrales impliquées.
L’endormissement : un phénomène complexe
Le sommeil ne survient pas qu’en raison d’un état de fatigue. L’hygiène de vie, les consommations (alcool, substances excitantes…), l’environnement immédiat (lumière, bruit…) peuvent influencer la capacité d’un individu à s’endormir. Mais biologiquement, cette phase nécessite aussi la convergence de plusieurs acteurs :
– des processus homéostasiques, processus physiologique qui permet de maintenir un équilibre nécessaire à un fonctionnement normal, qui accroissent le besoin du sommeil à mesure que la période de veille se prolonge ;
– des processus circadiens, qui visent à synchroniser l’organisme et le sommeil sur l’alternance jour-nuit.
Les processus homéostasiques, maître du sommeil lent
La régulation du sommeil est d’abord sous la dépendance de certains facteurs produits au cours de la journée (interleukine-1, prostaglandine D2, somatolibérine…), dont la pression favoriserait progressivement la survenue du sommeil. Parmi eux, l’ adénosine jouerait un rôle central. Produit lors de l’éveil, son accumulation favoriserait le sommeil. En effet, elle inhiberait progressivement le fonctionnement cérébral jusqu’au déclenchement du sommeil. Dès lors, l’adénosine est progressivement éliminée au cours de la nuit. Expérimentalement, plus la dette de sommeil est importante, plus le taux en adénosine est élevé et plus les ondes du sommeil lent profond sont intenses : il s’agirait d’un mécanisme permettant au cerveau de rattraper son retard.
Le système circadien, maître de l’horloge biologique
Physiologiquement, le rythme circadien est propre à chacun : avec une rythmicité proche de 24 heures, il varie en réalité de quelques dizaines de minutes d’un individu à l’autre. Plusieurs facteurs interviennent donc pour le réguler plus finement, parmi lesquels :
Les cellules ganglionnaires à mélanopsine
Le cyclage jour-nuit de notre organisme dépend des cellules ganglionnaires à mélanopsine de la rétine. En pratique, on sait aujourd’hui que celles-ci n’ont qu’un rôle partiel sur l’induction du sommeil. En effet, les expériences conduites sur des sujets isolés de la lumière du soleil durant plusieurs jours consécutifs montrent qu’une alternance veille-sommeil proche de celle vécue habituellement subsiste malgré tout. Le déclenchement du sommeil est donc un phénomène endogène qui est maintenu en l’absence de lumière. Les cellules ganglionnaires à mélanopsine ont essentiellement pour rôle de transmettre l’information sur l’alternance jour-nuit à des structures cérébrales impliquées dans d’autres fonctions. Néanmoins, l’usage tardif d’écrans ou de lumière LED, riches en lumière bleue, stimule ces cellules et perturbe le sommeil.
La mélatonine
L’induction du sommeil est également sous la dépendance hormonale de la mélatonine. Appelée communément hormone du sommeil, la mélatonine est produite en situation d’obscurité, en début de nuit, par la glande pinéale (ou épiphyse), située à l’arrière de l’hypothalamus. A l’inverse, lorsque les cellules rétiniennes perçoivent la lumière, sa synthèse est inhibée. Lorsqu’elle est libérée en début de nuit, elle favorise le déclenchement du sommeil. Avec le vieillissement, la production de mélatonine est de moins en moins efficace. C’est ce qui explique de nombreux troubles du sommeil liés à l’âge.
Les gènes horloge
Une quinzaine de gènes horloges (CLOCK, BMAL, Per, Cry, Reverb…) ont une expression qui est modulée selon l’information reçue par les cellules rétiniennes, la mélatonine et d’autres facteurs synchroniseurs (activité physique, prise alimentaire…). Exprimés au niveau des noyaux suprachiasmatiques, ils conduisent à la transmission de messages à plusieurs horloges secondaires situés au niveau cérébral, permettant la régulation du sommeil, mais aussi de nombreuses autres fonctions rythmées par le cycle circadien (production de cortisol, d’ACTH, d’hormone de croissance…). Expérimentalement, la destruction des noyaux suprachiasmatiques chez l’animal permet de maintenir l’alternance entre veille et sommeil, mais selon un rythme désorganisé et saccadé au cours de la journée. Notre horloge interne fonctionnerait donc comme un organisateur des moments de veille et de sommeil.
Le sommeil, c’est la santé

AS Urrila et coll. Sci Rep, 2017

FP Cappuccio et coll. Diabetes Care, 2010

AA Prather et coll. Sleep, 2015
Le sommeil représente la forme la plus aboutie du repos. Il permettrait ainsi à l’organisme de récupérer, que ce soit sur le plan physique ou mental. Dans ce processus, le sommeil lent jouerait un rôle particulier puisque les ondes lentes sont d’autant plus intenses et élevées que la quantité ou la qualité du sommeil ont été mauvaises la nuit précédente. Le sommeil permettrait aussi de réduire le métabolisme et de préserver l’énergie (rôle homéostasique). Ainsi, la température corporelle s’abaisse autour de 36°C durant la nuit.
A la fin du 19e siècle, les premières expériences de privation du sommeil conduites sur plus de trois jours ont notamment décrit une altération des capacités mnésiques et du temps de réaction motrice, des hallucinations et une baisse de la température corporelle. Celles qui ont été conduites par la suite ont confirmé le rôle du sommeil dans les phénomènes de concentration, d’apprentissage, de mémorisation ou d’orientation.
Dès les années 1980, il est devenu de plus en plus évident que le sommeil n’était pas uniquement utile à la mémoire et à la récupération. Son rôle serait particulièrement important pour la santé. Grâce aux travaux étudiant l’altération de l’état de santé des personnes souffrant de troubles du sommeil, il a été possible de mettre en exergue qu’une mauvaise qualité/quantité de sommeil accentue le risque d’irritabilité, de symptômes dépressifs, mais aussi de prise de poids, d’hypertension ou d’infection. Des données qui permettent de conforter l’idée communément admise selon laquelle les personnes fatiguées ont un risque accru de tomber malade…
Sommeil, maturation cérébrale et apprentissage
Les données d’imagerie décrivent qu’un nouvel apprentissage est associé, au cours de la nuit suivante, à l’augmentation du nombre d’épines dendritiques, les excroissances qui connectent les neurones adjacents entre eux et facilitent le passage d’informations de l’un à l’autre. Ces mécanismes expliquent probablement pourquoi un nouveau-né a besoin de dormir deux fois plus longtemps qu’un adulte.
Lisez la deuxième partie de cet article
yogaesoteric
17 décembre 2018
Also available in:

