CRIIGEN — Note d’expertise grand public sur les vaccins ayant recours aux technologies de modifications génétiques des organismes (I)
Nous reproduisons ici de la « Note d’expertise grand public sur les vaccins ayant recours aux technologies OGM » écrite et publiée en septembre 2020 par le Dr Christian Vélot, généticien moléculaire à l’Université Paris-Saclay et Président du Conseil scientifique du CRIIGEN.
I. Rappels de quelques notions et de terminologie
1. La cellule, l’ADN, l’ARN, les protéines
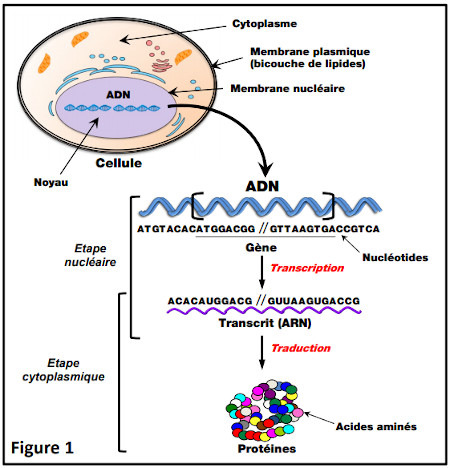
L’ADN est le support de l’information génétique. Il est localisé dans un compartiment particulier de chaque cellule de l’organisme, le noyau, lequel est séparé du reste de la cellule (le cytoplasme) par une membrane biologique appelée membrane nucléaire et contenant des ouvertures (les pores nucléaires). Chaque cellule est elle-même délimitée par une membrane biologique appelée membrane plasmique et constituée d’une bicouche de lipides (Figure 1). L’information génétique est identique dans toutes les cellules du corps d’un même individu, et est répartie sur plusieurs entités appelées chromosomes. Chez les humains, le nombre de chromosomes différents est de 23. Ils sont présents en double dans chaque cellule (à l’exception des spermatozoïdes et des ovules où ils ne sont qu’en un seul exemplaire), soit 46 chromosomes (23 paires comprenant chacune un chromosome provenant du père et l’autre provenant de la mère). L’ensemble des chromosomes d’un organisme vivant constitue son génome. Chaque chromosome est constitué de deux brins parallèles entourés autour d’un axe pour former une double hélice : la double hélice d’ADN. Chacun des deux brins de cette double hélice est lui-même constitué de l’enchaînement de quatre molécules plus petites, les nucléotides, que l’on désigne par leurs initiales respectives, c’est-à-dire quatre lettres : A, G, C, T (Figure 1).
Les gènes sont des segments de chromosomes (des morceaux de séquences en quatre lettres) qui détiennent une (ou des) information(s) biologique(s) permettant aux cellules de fonctionner. Un même gène chez une même espèce peut exister sous différentes formes, avec de légères modifications de séquence : ce sont les différents allèles d’un gène. Les allèles de l’ensemble des gènes d’un individu déterminent son génotype. Pour l’essentiel des gènes que nous connaissons aujourd’hui (et qui ne représentent qu’une toute petite partie d’un génome), les gènes détiennent le secret de fabrication des protéines. Les protéines sont de grosses molécules constituées par l’enchaînement linéaire, non pas de quatre, mais de 20 molécules différentes : les acides aminés (Figure 1). Le passage d’un gène à une protéine correspond donc au passage d’un langage en quatre lettres (A, G, C, T : le langage génétique) à un langage en 20 lettres (les 20 acides aminés : le langage protéique). Ce processus s’appelle d’ailleurs la traduction.
Toutefois, le passage du gène à la protéine n’est pas direct : il nécessite une molécule intermédiaire, constituée elle aussi de l’enchaînement de quatre nucléotides (langage génétique A, G, C, U au lieu de A, G, C, T) et formée d’un seul brin (simple hélice). Il s’agit d’une molécule d’ARN, appelée aussi transcrit car elle est le résultat d’un processus appelé transcription (passage de l’ADN à l’ARN) qui a lieu dans le noyau. Cette molécule d’ARN va ensuite sortir du noyau par les pores nucléaires pour rejoindre le cytoplasme où elle sera traduite en protéine. L’expression d’un gène codant une protéine se fait donc en deux étapes, la première (nucléaire) étant la transcription, et la seconde (cytoplasmique) la traduction (Figure 1).
Précisons que tous les gènes ne codent pas des protéines. Autrement dit, l’expression des gènes ne comprend pas toujours une étape de traduction mais, en revanche, passe systématiquement par une étape de transcription. Les transcrits ne sont donc pas toujours des intermédiaires mais peuvent être les produits finis de l’expression génique.
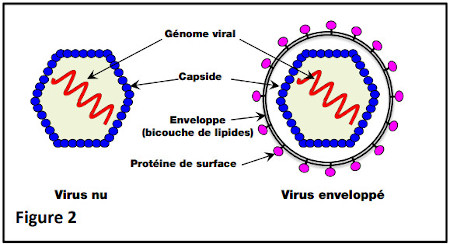
Les virus sont des agents infectieux constitués d’une coque protéique appelée capside, constituée de la juxtaposition d’un grand nombre d’exemplaires d’une protéine virale, et renfermant le matériel génétique du virus (Figure 2) qui est soit de l’ADN soit de l’ARN. De nombreux virus sont en plus entourés d’une enveloppe qui est constituée d’une bicouche de lipides correspondant à celle de la membrane plasmique de leurs cellules hôtes (les cellules qu’ils infectent) et contenant des protéines qui y sont enchâssées : les protéines de surface du virus (Figure 2). Les virus possédant une enveloppe sont appelés des virus enveloppés ; ceux n’en possédant pas sont les virus nus (Figure 2). Le virus SARS-CoV-2, responsable de la Covid-19, est un virus enveloppé, de même que le virus de la grippe ou le VIH, responsable du SIDA.
Les virus n’ont pas la capacité de se reproduire seuls et doivent nécessairement infecter des cellules hôtes dont ils détournent l’activité au profit de leur propre multiplication. Pour cela, les virus injectent leur matériel génétique dans les cellules qu’ils infectent. Celles-ci vont alors multiplier ce matériel génétique et exprimer les gènes viraux qu’il contient afin de produire en grand nombre les protéines virales. De nombreuses particules virales vont alors se reconstituer à l’intérieur de la cellule infectée.
Pour les virus nus, la reconnaissance des cellules hôtes se fait par l’intermédiaire des protéines de la capside qui vont interagir spécifiquement avec une ou plusieurs protéine(s) située(s) dans la membrane plasmique des cellules hôtes. Cette interaction permet l’encrage du virus à la surface de la membrane plasmique puis sa pénétration dans les cellules ainsi infectées. Dans le cas des virus enveloppés, la reconnaissance et l’encrage se fait par la protéine de surface, et la pénétration du virus par fusion entre l’enveloppe virale et la membrane plasmique de la cellule hôte.
Une fois à l’intérieur de la cellule infectée, le matériel génétique viral va y être pris en charge selon des mécanismes différents en fonction notamment de sa nature : ADN ou ARN.
Pour les virus à ADN, l’ADN viral est directement pris en charge par la machinerie de la cellule infectée afin de le répliquer et d’exprimer ses gènes pour produire les protéines virales. Dans un certain nombre de cas, l’ADN viral peut aussi s’intégrer dans le génome des cellules infectées (c’est notamment le cas du papillomavirus responsable de cancers de l’utérus).
Concernant les virus à ARN, on distingue deux grands cas de figure.
Pour certains virus à ARN, comme le VIH, l’ARN viral est d’abord transformé en ADN sous l’action d’une enzyme virale, la transcriptase inverse, injectée dans la cellule infectée avec l’ARN viral. Cette étape est donc l’inverse d’une transcription, qui, elle, consiste à faire de l’ARN à partir d’ADN (Figure 1). L’ADN viral ainsi obtenu pénètre dans le noyau par les pores nucléaires et s’intègre alors au génome des cellules infectées. Cette seconde étape, pour se faire avec une grande efficacité, nécessite à nouveau une enzyme virale : l’intégrase. La cellule infectée peut alors prendre en charge l’ADN viral comme s’il s’agissait du sien et le transcrire en un grand nombre d’exemplaires, certains des transcrits seront traduits afin de produire les protéines virales.
Pour d’autres virus à ARN, comme le SARS-CoV-2, l’ARN viral est directement pris en charge par la machinerie cellulaire pour le traduire et ainsi fabriquer les différentes protéines virales, dont l’enzyme nécessaire à la réplication en un grand nombre d’exemplaires de cet ARN. Il n’y a donc pas dans ce cas présence ou production d’ADN viral, et donc pas d’intégration du génome viral dans les cellules infectées. C’est aussi le cas du virus de la grippe même si son ARN viral ne peut être traduit directement par la machinerie cellulaire et doit d’abord être répliqué en une copie complémentaire grâce à une enzyme virale directement libérée dans la cellule avec l’ARN.
II. La vaccination
La vaccination a pour but de stimuler les défenses immunitaires d’un humain ou d’un animal vis-à-vis d’un agent infectieux en l’exposant volontairement à cet agent (sous une forme atténuée ou inactivée) ou à l’un de ses composants appelé antigène (généralement une protéine). Pour ce qui est des virus, la plupart des vaccins consiste jusqu’à aujourd’hui à injecter une forme atténuée (« vaccins vivants ») ou inactivée (« vaccins inactivés ») du virus entier.
L’atténuation est obtenue principalement selon deux procédés. Le premier consiste à faire passer le virus sur des cultures de cellules d’une autre espèce : il reste alors immunisant mais ne peut plus se multiplier chez l’homme. C’est le procédé utilisé notamment pour les vaccins contre la rougeole, les oreillons, la rubéole, la varicelle. Le second procédé consiste à utiliser soit des mutants thermosensibles du virus, soit des virus adaptés au froid après passages successifs en cultures cellulaires à basse température : ces virus ont alors une capacité très réduite à se multiplier à 37°C (et donc chez l’humain). Ce procédé a été utilisé notamment pour un ancien vaccin contre le virus de la grippe administré par voie nasale (Fluenz®, aujourd’hui retiré) et pour le vaccin contre le virus respiratoire syncytial (VRS). Les principaux inconvénients sont d’une part les risques d’apparition de révertants du virus (souche sauvage) par recombinaison entre la souche vaccinale et une souche pathogène présente chez l’hôte vacciné (c’est-à-dire une ré-acquisition de pathogénicité par la souche vaccinale initialement atténuée), et d’autre part une contre-indication chez les personnes immunodéprimées ou chez les femmes enceintes en raison d’un risque d’atténuation insuffisante pour ces personnes.
L’utilisation de virus inactivés est donc plus sûre (mais pas dénuée de tout risque pour autant : voir section IV.1.). L’inactivation est soit chimique (traitement au formaldéhyde essentiellement), soit physique (chaleur ou irradiation). Ce type de vaccins dits « inactivés » concerne notamment la grippe, l’hépatite A, la poliomyélite, la rage. Leur désavantage est qu’ils provoquent une réponse immunitaire plus faible, ce qui nécessite des injections multiples et répétées, ainsi que l’utilisation d’adjuvants tels que l’aluminium ajoutés pour potentialiser l’effet immunogène du vaccin, et susceptibles d’engendrer des effets toxiques.
Depuis les années 90, des vaccins sont obtenus en ayant recours aux biotechnologies. Actuellement, cela consiste principalement à faire produire à des cellules cultivées en laboratoire (essentiellement des cellules de bactéries, de levures ou de champignons filamenteux) une protéine d’un agent infectieux (antigène). Il s’agit donc de cellules transgéniques dans le génome desquelles a été inséré le gène de l’agent infectieux codant cet antigène. L’antigène en question est alors purifié et associé à divers adjuvants pour élaborer un vaccin qui sera injecté aux patients. C’est notamment le cas du vaccin Engerix™-B contre l’hépatite B où la protéine de surface de ce virus a été produite dans des cellules d’une levure transgénique (levure de boulanger) exprimant le gène viral en question. Le coût de production est relativement élevé en raison notamment de l’étape de purification de l’antigène à partir des cellules transgéniques qui le produisent.
Enfin, de nouvelles stratégies faisant également appel aux biotechnologies sont en cours de développement depuis plusieurs années. Elles consistent à faire produire l’antigène de l’agent infectieux directement par les cellules de l’hôte (de la personne que l’on cherche à vacciner) en lui injectant l’ADN ou l’ARN codant la protéine virale en question.
L’introduction de ce matériel génétique dans les cellules de l’hôte nécessite d’utiliser des « véhicules » appelés vecteurs. Ces vecteurs sont soit dérivés de petites molécules d’ADN circulaire bactérien, appelées plasmides, et dans lesquelles a été introduit l’ADN viral codant la protéine antigénique, soit des nanoparticules de lipides dans lesquelles sont emprisonnées l’ARN codant cet antigène, soit encore des virus génétiquement modifiés dits « désarmés », c’est-à-dire rendus notamment incapables de se répliquer par élimination d’une partie de leur matériel génétique (ADN ou ARN), lequel est remplacé par le matériel génétique d’intérêt que l’on souhaite introduire dans les cellules de l’hôte. Dans ce dernier cas, on utilise alors la capacité naturelle des virus en question à injecter le matériel génétique qu’ils contiennent dans les cellules humaines.
III. Les projets de vaccins contre la Covid-19
Selon la liste de l’Organisation Mondiale de la Santé (OMS) actualisée au 22 septembre 2020, 38 candidats vaccins font l’objet d’essais cliniques (de phase I, II ou III).
Six d’entre eux utilisent le virus inactivé, tous les autres reposent sur des approches biotechnologiques et consistent à injecter soit a) une protéine du virus (antigène) ; b) des particules pseudo-virales ; c) l’ADN ou l’ARN codant l’antigène.
a. Dans le cas où le vaccin consiste à injecter une protéine du virus, celle-ci est produite en laboratoire par des cellules transgéniques dans lesquelles a été introduit une construction génétique contenant le gène viral correspondant et permettant son expression en grande quantité dans les cellules en question. Ces cellules sont alors cultivées à grande échelle dans des fermenteurs (bioréacteurs) et la protéine est extraite des cellules et purifiée. Cela concerne 13 des 38 vaccins en cours d’essais
b. Une particule pseudo-virale (VLP en anglais : virus-like particle) est en fait la capside sans le génome viral, obtenue par l’assemblage spontané de la protéine de la capside elle-même produite en laboratoire dans des cellules transgéniques. Dans ce cas précis (1 seul des 38 vaccins testés), il s’agit de cellules de plantes.
c. Les 18 vaccins restants consistent donc à introduire du matériel génétique viral dans les cellules de la personne à vacciner (l’administration est essentiellement intramusculaire, voire intradermique dans deux des cas). Il s’agit soit d’ARN emprisonné dans des nanoparticules de lipides (6 cas), soit d’ADN inséré dans un plasmide (4 cas), soit encore d’ADN ou d’ARN délivré par un virus génétiquement modifié désarmé (8 cas).
Lisez la deuxième partie de cet article
