Vaccins anti-covid, sûrs et efficaces ? Avis du Conseil Scientifique, de la HAS, ce qu’en a fait la Commission Européenne (1)
Par Emma Kahn
L’industrie pharmaceutique s’est donc déjà lancée dans la production de centaines de millions de doses de vaccins anti-covid un peu partout dans le monde, dans le plus grand désordre. Peu importe que toute la communauté scientifique encore indépendante tire toutes les sonnettes d’alarme possibles, les firmes s’entêtent dans un productivisme démentiel simplement justifié par des messages publicitaires atterrants de nullité. Où sont leurs preuves d’efficacités ? Quels résultats ont-t-elles obtenu en matière de biosécurité s’agissant de ces produits ?

Résumé
Le CS a donné son avis en juillet 2020 pour fixer la « doctrine de la vaccination » : les incertitudes scientifiques qu’il soulève sont confrontées ici à ce qui est accessible à ce jour sur la sécurité et l’efficacité des futurs vaccins. La CE a d’ores et déjà signé les contrats avec les fabricants avant évaluation correcte de ces critères. Ces contrats sont rapidement exposés ici. Nous verrons que les exigences de transparence sont loin d’être réalisées. Comme déjà exposé, le danger d’ADE (aggravation de l’infection par les anticorps induits par le vaccin) est souligné par le CS. Les dangers généraux et spécifiques de chaque type de vaccin sont exposés ici (vaccins à ADN, à ARNm, à protéine recombinante, à vecteur viral). Les défauts manifestes dans les essais cliniques montrent que ceux-ci sont loin d’être transparents et ne répondent pas aux questions essentielles : les vaccins seront-ils capables d’arrêter la transmission du virus et d’éviter les formes graves ? Les effets secondaires sont insuffisamment évalués dans les essais et la vaccino-vigilance post-commercialisation n’est pas adaptée pour les identifier.
Introduction
En juillet 2020 le Conseil Scientifique (CS) a émis un long avis, assez honnête et documenté, sur les futurs vaccins anti-covid. En novembre 2020, la Haute Autorité de Santé (HAS) lance une enquête pour assurer la transparence dans la campagne de vaccination.
Mais la Commission Européenne (CE) outrepasse ces futilités : elle vient de finir de signer six contrats aussi secrets que faramineux avec les fabricants de vaccins, et ceci pour un nombre de doses correspondant à la vaccination complète de 1,2 milliards d’individus !
La fabrication de ces vaccins a déjà commencé avant la fin (et même parfois le début !) des essais cliniques de phase III. Profitons de cette magnifique transparence pour examiner à la loupe les problèmes de sécurité et d’efficacité des futurs vaccins. Le Conseil Scientifique a donné son avis le 9 juillet 2020 sur la future campagne de vaccination anti-Covid-19.
Le Conseil Scientifique ne recommande pas d’obligation vaccinale mais n’envisage pas une stratégie vaccinale fondée sur des choix purement individuels, notez la nuance subtile. (1)
D’un point de vue scientifique, les questions soulevées par le CS n’ont pas reçu de réponses satisfaisantes. La procédure accélérée de mise sur le marché ne permet pas de répondre aux incertitudes scientifiques sur l’efficacité et la sécurité des vaccins. Les contrats ont été signés par la CE et sont valables pour la France. Les pays membres ne disposent que d’une faible marge de manœuvre dans l’application de la politique vaccinale. Les contrats sont secrets, on ne connaît pas les négociateurs (2).
Aspects généraux
• Le Conseil Scientifique demande la gratuité du vaccin :quel sera le coût pour la Sécurité Sociale une fois ajouté au coût des tests PCR et antigéniques dont l’utilité en Santé Publique n’est pas démontré (voir l’avis de la Cour d’Appel du Portugal à ce sujet ; (3)
• Selon le CS, la tenue du registre vaccinal sera adossée au DMP (dossier médical partagé) : il y a un problème de confidentialité des données ; (4)
• Le CS souligne la difficulté faire accepter aux professionnels de santé de se vacciner eux-mêmes pour mettre en confiance le public : en effet, peu de professionnels se vaccinent contre la grippe étant donnés les doutes sur l’utilité et l’efficacité du vaccin. La couverture vaccinale contre la grippe chez ceux-ci est estimée à 34,8 % ; (5)
• D’après le CS, la communication doit être transparente sur les procédures accélérées de mise sur le marché, sur les incertitudes et les fondements scientifiques.
La communication se fait actuellement par communiqués de presse ou communiqué boursier par les fabricants eux-mêmes (voir Biontech 18 novembre 2020, qui prétend publier des résultats préliminaires d’une étude clinique randomisée (ECR), non revus par les pairs. (6)
Teneur des contrats signés par l’union Européenne avec les fabricants de vaccins – Etat des lieux au 24 novembre 2020
Ces contrats ne sont pas publics, voici ce qu’on sait des commandes signées : (7)
• Astra Zeneca :300 millions de doses avec option de 100 millions supplémentaires ;
• Sanofi-GSK : 300 millions ; Les états pourront donner les doses aux pays à faible revenu. Le protocole est secret mais ce vaccin repose sur la technique protéine recombinante (spike) associée à un adjuvant pour en augmenter l’immunogénicité ; Ce sera l’adjuvant GSK, AS03 utilisé dans le Pandermix de 2009 contre la grippe H1N1 soupçonné d’avoir provoqué des narcolepsies (ce qui expliquerait qu’ils soit destiné aux pays pauvres ?) De plus la fabrication est plus longue que celle des vaccins ARNm ou ADN, il sera donc disponible plus tard que les autres ;
• Janssen, Johnson et Johnson : vaccins monodoses commandés pour 200 millions de personnes + 200 millions supplémentaires ;
• CureVac : 225 millions de doses et 180 millions doses supplémentaires ;
• Pfizer : 200 millions de doses et 100 millions supplémentaires ;
• Moderna : 80 millions de doses et 80 millions doses supplémentaires, signé le 24 novembre 2020. (8)
Si on tient compte des protocoles à 2 doses (tous sauf Janssen Johnson et Johnson), l’UE (448 millions d’habitants) a ainsi commandé des vaccins pour 1,182 milliards d’individus.
Pourquoi autant ? Serait-ce que les mutations du virus sont intégrées dans le projet et les commandes prévues pour vacciner plusieurs fois les mêmes personnes avec des vaccins adaptés à l’évolution du virus ?
Le CS demande de mettre l’accent sur l’aspect altruiste des vaccins, pour cela il faut un vaccin stérilisant permettant d’interrompre la transmission du virus : Comment les vaccins pourraient-ils être altruistes puisque les vaccins ne seront pas stérilisants, ceci n’est pas envisagé dans les études cliniques. (9)
Selon un virologiste renommé (communication personnelle), « l’immunité stérilisante est exceptionnellement observée dans les viroses aigües. Le tractus respiratoire supérieur est classiquement décrit comme un ” sanctuaire ” viral où l’immunité est peu efficace. C’est bien pour cela qu’il n’y a pas de protection immunitaire solide ni de vaccin efficace contre les ” rhumes „. Une immunité antivirale capable de bloquer le rhume et donc la contagion qui va avec n’a jamais été observée. »
Selon que l’on utilisera un vaccin stérilisant ou protecteur les populations ciblées sont différentes.
Comme on ne sait pas si les futurs vaccins seront stérilisants (empêcheront totalement l’infection bénigne du type des rhumes) ou n’empêcheront pas la diffusion, il est impossible de cibler les populations prioritaires !
Aspects scientifiques
Le Conseil Scientifique a demandé une communication transparente, or celle-ci se fait actuellement par communiqués de presse boursiers par les fabricants eux-mêmes. (10)
AstraZeneca a publié dans le Lancet le 18 novembre 2020, sous la forme d’un résultat préliminaire d’étude clinique, ce qui est n’en fait qu’un document publicitaire. (11) On y voit que l’étude n’est qu’en simple-aveugle, le placebo n’en est pas un puisque c’est le vaccin anti-méningocoque très immunogène. Fait rédhibitoire, le protocole a été changé en cours d’essai, au départ il s’agissait d’un vrai placebo salin. Tout ceci invalide complètement les prétendus résultats de l’essai.
Celui-ci a inclus des personnes de plus de 70 ans mais elles ont été sélectionnées en bonne santé, ce qui n’est pas le cas des sujets à risques ciblés par le vaccin.
• Le tableau donnant la liste des graves effets secondaires est très inquiétant : On ne peut y distinguer les effets secondaires occasionnés chez les personnes vaccinées de ceux observés chez les personnes ayant reçu le placebo, y aurait-il quelque chose à cacher ?
• Comme attendu aucun effet secondaire n’est relié au vaccin par les investigateurs ;
• Il y a une majorité d’effets secondaires graves chez les plus de 70 ans, CONTRAIREMENT à ce qui est écrit dans le titre et le résumé !
• La plupart des effets secondaires graves sont observés pour des participants dont les données sur l’injection de la deuxième dose ne sont pas communiquées : pourquoi ? La première dose aurait-elle provoqué des effets si préoccupants que la deuxième dose n’aurait pas été injectée ?
• En ce qui concerne les effets secondaires « bénins » attendus, on observe plus de réactions indésirables avec le vaccin qu’avec le « placebo » déjà très immunogène !
Cerise sur le gâteau, Astra-Zeneca vient d’admettre avoir commis une erreur dans son protocole qui fausserait les résultats mirobolants d’efficacité : une partie non négligeable des participants a reçu une demi-dose de vaccin au lieu de la dose prévue ; comment faire confiance à des essais aussi mal menés et aux publications officielles qui en sont faites ? (12)
Le CS souligne l’intérêt d’explorer les réponses immunes cellulaires : l’analyse de la diversité des réponses et leur persistance nécessite des études complémentaires. Il n’est pas prévu d’explorer ces réponses dans la plupart des protocoles d’essais cliniques publiés et en effet les études cliniques et pré-cliniques prennent ordinairement entre 5 et 15 ans, or ici c’est du « fast track » !
Le Conseil Scientifique souligne que l’immunité croisée avec les coronavirus de rhume banal est détectée chez 40 à 60% des non exposés à la Covid-19, il n’est pas tenu compte de ce fait dans la prévision de campagnes massives et non ciblées de vaccination (13). Il rappelle que l’ADE ou VAED (Vaccine Associated Enhanced Disease ou aggravation de la maladie par le vaccin) est suggéré par les modèles animaux.
Pour l’instant il n’y a pas de corrélat de protection connu, mais il est postulé que les vaccins devraient induire des anticorps neutralisants contre la protéine S ou son RBD (domaine de liaison au récepteur cellulaire), une réponse T cell type Th1, non de type Th2, un taux élevé d’anticorps atteint rapidement pour éviter l’ADE et le VAED. Les vaccins devront également éviter les adjuvants de type Th2.
Tout ceci pose problème : Les études cliniques en cours n’évaluent pas du tout le type d’immunité conférée par les vaccins mais seulement le taux d’anticorps contre la spike protéine.
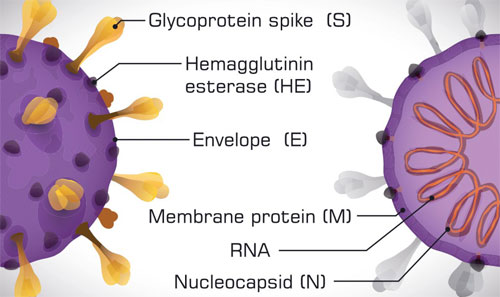
Il faudra démontrer ces potentiels des vaccins en essais cliniques et évaluer leur valeur protectrice sur des modèles animaux., vérifier l’absence de VAED par des analyses histopathologiques sur les tissus pulmonaires. Tous les efforts doivent être engagés pour une analyse plus précise des mécanismes potentiels d’ADE.
Les études cliniques n’évaluent pas non plus ces points, pas d’analyse de l’ADE (Voir : Doshi Peter, op. Cit.). De plus les modèles animaux choisis pour les essais ne sont pas adaptés. (14)
Selon le Conseil Scientifique, la vaccination des personnes ayant déjà été infectées sera possible : il affirme qu’il est inutile de faire une sérologie préalable car pas il n’y aucun problème envisagé : aucune étude n’est jamais venue en soutien d’une telle cette assertion !
Le CS demande de profiter de la vaccination anti-covid pour mettre à jour le calendrier vaccinal, vaccin grippe et pneumocoque, mais on rappelle que la vaccination anti-grippale est soupçonnée fortement de favoriser les infections à coronavirus chez les adultes (15) et les enfants (16)(17).
Autres remarques du Conseil Scientifique
Le CS rappelle les problèmes généraux concernant la vaccination : réponses immunitaires faibles chez personnes vaccinées, doute sur efficacité des vaccins, accidents rares mais désastreux, tout ça pouvant annihiler la confiance. Dans le cas particulier covid des doutes sont émis sur :
• L’efficacité,
• La sécurité,
• La capacité immunisation,
• La durée immunisation,
• Les possibles mutations réduisant protection vaccinale,
• Les possibles effet secondaires (dont « les ” antibody-dependent enhancement (ADE) effects ” observés pour certains coronavirus, responsables de rechutes graves de la maladie lors d’une deuxième infection. »)
Concernant l’ADE et VAED : (risque d’aggravation de l’infection suite à la vaccination) Voir l’article complet paru dans le Vidal « Vaccins contre la COVID-19 : doit-on s’inquiéter du risque de maladie aggravée chez les personnes vaccinées ? » (18)
Concernant les doutes sur l’efficacité et la sécurité des vaccins : Auparavant les essais précliniques et cliniques pour les nouveaux vaccins duraient de 5 à 15 ans, ils sont ici accélérés sur moins d’un an (19). Les contrats signés par l’UE (et valables pour la France) nous apprennent quels vaccins seront fabriqués et sont déjà précommandés.
Le fait que la production des vaccins a commencé bien avant les résultats ou même le début des études cliniques exerce une pression intolérable sur les États pour les forcer à commander cette production. (19b)
Lire la deuxième partie de cet article
Notes et sources
(1) https://solidarites-sante.gouv.fr/IMG/pdf/avis_vaccins_9_juillet_2020_-_care_-_conseil_scientifique_-_comite_vaccin.pdf
(2) https://www.francetvinfo.fr/sante/maladie/coronavirus/vaccin/vaccins-contre-le-covid-19-les-eurodeputes-demandent-a-la-commission-europeenne-de-la-transparence-sur-les-contrats-passes-avec-les-labos_4187763.html
(3) https://drive.google.com/file/d/1t1b01H0Jd4hsMU7V1vy70yr8s3jlBedr/view
(4) https://www.lemonde.fr/idees/article/2019/12/10/l-exploitation-de-donnees-de-sante-sur-une-plate-forme-de-microsoft-expose-a-des-risques-multiples_6022274_3232.html
(5) https://www.santepubliquefrance.fr/determinants-de-sante/vaccination/articles/etudes-de-couverture-vaccinale-chez-les-professionnels-de-sante-des-etablissements-de-sante-et-ehpad-saison-2018-2019
(6) https://www.pfizer.com/news/press-release/press-release-detail/pfizer-and-biontech-conclude-phase-3-study-covid-19-vaccine
(7) https://ec.europa.eu/commission/presscorner/detail/fr/ip_20_2136
(8) https://www.leparisien.fr/societe/coronavirus-conseil-de-defense-et-allocution-de-macron-ce-mardi-suivez-notre-direct-24-11-2020-8410102.php
(9) Will covid-19 vaccines save lives? Current trials aren’t designed to tell us BMJ 2020; 371 :m4037
Le monde a parié sur la production de vaccins comme solution à la pandémie, mais les essais ne visent pas à répondre aux questions que beaucoup pourraient supposer qu’ils sont.
(10) https://www.pfizer.com/news/press-release/press-release-detail/pfizer-and-biontech-conclude-phase-3-study-covid-19-vaccine
(11) Ramasamy MN, Minassian AM, Ewer KJ, Flaxman AL, Folegatti PM, Owens DR, Voysey M, Aley PK, Angus B, Babbage G, Belij-Rammerstorfer S, Berry L, Bibi S, Bittaye M, Cathie K, Chappell H, Charlton S, Cicconi P, Clutterbuck EA, Colin-Jones R, Dold C, Emary KRW, Fedosyuk S, Fuskova M, Gbesemete D, Green C, Hallis B, Hou MM, Jenkin D, Joe CCD, Kelly EJ, Kerridge S, Lawrie AM, Lelliott A, Lwin MN, Makinson R, Marchevsky NG, Mujadidi Y, Munro APS, Pacurar M, Plested E, Rand J, Rawlinson T, Rhead S, Robinson H, Ritchie AJ, Ross-Russell AL, Saich S, Singh N, Smith CC, Snape MD, Song R, Tarrant R, Themistocleous Y, Thomas KM, Villafana TL, Warren SC, Watson MEE, Douglas AD, Hill AVS, Lambe T, Gilbert SC, Faust SN, Pollard AJ; Oxford COVID Vaccine Trial Group. Safety and immunogenicity of ChAdOx1 nCoV-19 vaccine administered in a prime-boost regimen in young and old adults (COV002) : a single-blind, randomised, controlled, phase 2/3 trial. Lancet. 2020 Nov 18:S0140-6736(20)32466-1. doi: 10.1016/S0140-6736(20)32466-1. Epub ahead of print. PMID: 33220855.
(12) https://www.fiercebiotech.com/biotech/astrazeneca-probes-mistake-behind-90-covid-vaccine-efficacy
(13) Covid-19 : Do many people have pre-existing immunity ? Doshi Peter. Covid-19 : Do many people have pre-existing immunity ? BMJ 2020 ; 370 :m3563
(14) Kanduc, D., Shoenfeld, Y. Molecular mimicry between SARS-CoV-2 spike glycoprotein and mammalian proteomes: implications for the vaccine. Immunol Res 68, 310–313 (2020).
(15) https://www.ncbi.nlm.nih.gov/pubmed/31607599
(16) Benjamin J. Cowling1, Vicky J. Fang1, Hiroshi Nishiura1,2, Kwok Hung Chan3, Sophia Ng1, Dennis K. M. Ip1, Susan S. Chiu4, Gabriel M. Leung1, J. S. Malik Peiris1,5 Increased risk of non influenza respiratory virus infections associated with receipt of inactivated influenza vaccine
(17) https://www.aimsib.org/2020/09/27/vaccin-anti-grippal-et-facilitation-de-linfection-par-les-anticorps/
(18) Vaccins contre la COVID-19 : doit-on s’inquiéter du risque de maladie aggravée chez les personnes vaccinées ?
(19) https://www.franceculture.fr/sciences/vaccin-contre-le-covid-19-au-coeur-des-recherches-de-sanofi
(19b) Odile Launay, août 2020, https://www.franceinter.fr/societe/covid-19-pour-l-instant-nous-n-avons-pas-la-preuve-de-l-efficacite-ni-de-l-innocuite-des-vaccins
yogaesoteric
14 janvier 2021
